Il Derma come Epicentro della Discromia Cutanea: Un'Analisi Multifattoriale
Meccanismi di stress ossidativo, inflammaging e senescenza cellulare alla base della pigmentazione irregolare
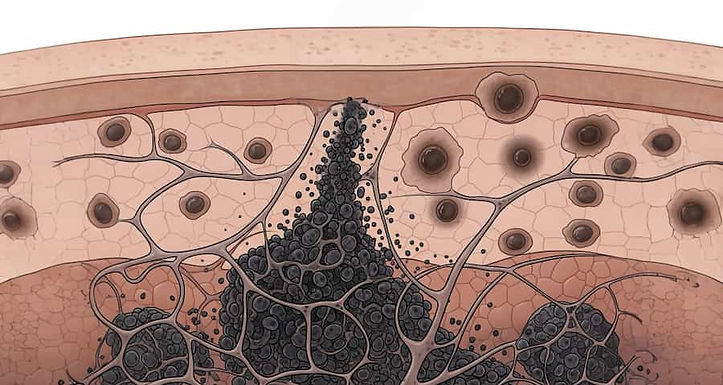
La discromia cutanea, che si manifesta attraverso macchie e un colorito non uniforme, rappresenta una condizione complessa che affonda le sue radici in una serie di reazioni a catena a livello del derma.
Questo articolo tecnico-scientifico si propone di delineare i meccanismi biochimici interconnessi – ossidativi, infiammatori, strutturali e vascolari – che conducono a uno stato di iperpigmentazione cronica. L'analisi dettagliata dei processi di stress ossidativo, infiammazione cronica (o "inflammaging"), senescenza fibroblastica e disregolazione della matrice nel derma è fondamentale per comprendere la fisiopatologia della pigmentazione irregolare e la centralità del derma in questo processo.
Lo Squilibrio Redox e l'Innesco dell'Infiammazione Cronica (Inflammaging)
Il processo patologico alla base delle discromie cutanee ha inizio con un accumulo eccessivo di molecole dannose quali i radicali liberi (ROS) e il perossinitrito.
Questo squilibrio ossidativo è indotto da diversi fattori, tra cui l'esposizione ai raggi UV, un'alterata funzione cellulare e uno stato infiammatorio di fondo. I radicali liberi esercitano un'azione dannosa sul DNA, sulle proteine e sulle membrane delle cellule del derma, in particolare sui fibroblasti. In risposta a tale danno, le cellule attivano specifici "fattori di emergenza" come NF-kB e AP-1, che a loro volta stimolano la produzione di sostanze pro-infiammatorie e di enzimi deputati alla degradazione della matrice cutanea. Questo meccanismo auto-alimentante di stress e infiammazione è centrale nella spirale che porta alla discromia.
Senescenza Fibroblastica e Secrezione del Fenotipo Pro-Pigmentogeno (SASP)
I fibroblasti, cellule fondamentali per la costruzione del derma, subiscono un progressivo danno che li conduce a uno stato di senescenza.
Tale condizione comporta l'arresto della loro capacità proliferativa e l'accumulo di lipofuscina, un pigmento di scarto di colore bruno che contribuisce all'aspetto spento del colorito cutaneo. Inoltre, i fibroblasti senescenti non sono più in grado di riparare la matrice extracellulare e, contestualmente, iniziano a secernere in grandi quantità sostanze infiammatorie, note collettivamente come Senescence-Associated Secretory Phenotype (SASP). Queste sostanze alterano il comportamento delle cellule circostanti, inclusi i melanociti, stimolandoli a una produzione disordinata e irregolare di melanina.
Degradazione della Matrice Extracellulare e Alterazione della Meccanotrasduzione
La struttura di sostegno del derma, composta principalmente da collagene, elastina e glicosaminoglicani, viene progressivamente degradata da enzimi della famiglia delle metalloproteinasi (MMP), la cui attività è indotta dallo stato infiammatorio. Le fibre di collagene, normalmente lunghe e ordinate, vengono frammentate in segmenti corti e disorganizzati, mentre l'elastina subisce frammentazione e raggrumamento, compromettendo la trasparenza della pelle. In situazioni di elevata esposizione solare, può verificarsi la formazione di ammassi di elastina danneggiata (solarelastosi), che conferiscono alla pelle un colorito giallo-marrone. La diminuzione delle molecole igroscopiche determina una perdita di spessore e idratazione, riducendo la capacità della pelle di riflettere la luce in modo omogeneo.
Tale danneggiamento e l'indurimento della matrice, spesso a causa di processi come la glicazione, influenzano anche i segnali meccanici percepiti dalle cellule. Fibroblasti e melanociti, attraverso recettori specifici, "sentono" questa aumentata rigidità; in risposta, i fibroblasti invecchiano più rapidamente e incrementano la secrezione di sostanze pro-pigmentazione, instaurando un circolo vizioso dove le aree più rigide diventano anche quelle più pigmentate
Disfunzione del Microcircolo e Ruolo dell'Ipossia nell'Iper-melanogenesi
L'infiammazione cronica e lo stress ossidativo compromettono l'efficienza dei piccoli vasi sanguigni del derma. Le pareti dei capillari tendono a ispessirsi e alcuni vasi possono chiudersi, determinando la formazione di aree con ridotto apporto di ossigeno (ipossia locale). Questa ipossia "a chiazze" funge da stimolo per l'attivazione di molecole, come HIF-1α, che promuovono ulteriormente la pigmentazione in specifiche zone, contribuendo alla disomogeneità del colorito. La fragilità vascolare può inoltre causare il deposito di ferro, il quale accentua l'intensità delle macchie scure.
Il Crosstalk Neuro-Infiammatorio e il Ruolo dei Mastociti
Le fibre nervose cutanee, quando sottoposte a stress, giocano un ruolo attivo nell'aggravamento del problema. Il rilascio di specifiche molecole da parte di queste fibre nervose contribuisce all'incremento dell'infiammazione locale e stimola i mastociti a liberare ulteriori sostanze pro-infiammatorie. Questo crosstalk neuro-infiammatorio amplifica significativamente il processo patologico che può evolvere verso la formazione di pigmentazioni cutanee stabili.
Deficit dei Sistemi di Proteostasi e Accumulo di Lipofuscina
In presenza di un sovraccarico dei sistemi di pulizia cellulare, quali l'autofagia e il proteasoma, si verifica un accumulo di proteine danneggiate e di frammenti di elastina. Queste molecole agiscono come "segnali di allarme" endogeni (Damage-Associated Molecular Patterns o DAMPs), che attivano ulteriormente i meccanismi infiammatori. L'accumulo di lipofuscina, già menzionato in relazione ai fibroblasti senescenti, contribuisce in maniera significativa a conferire alla pelle un tono grigiastro o giallo-bruno, accentuando la percezione della discromia.
Un Modello Integrato di Disregolazione Pigmentaria Dermica
Le discromie cutanee e la pigmentazione irregolare non sono fenomeni superficiali, ma il risultato di una complessa interazione di processi biochimici che hanno origine e si amplificano nel derma. Lo stress ossidativo innesca un'infiammazione cronica che danneggia i fibroblasti, inducendone la senescenza e la produzione di fattori pro-pigmentogeni (SASP). Contemporaneamente, l'infiammazione degrada la matrice extracellulare, alterandone la struttura e la meccanotrasduzione, il che a sua volta stimola i melanociti a produrre melanina in modo disordinato.
La disfunzione microvascolare e l'ipossia locale creano aree di maggiore pigmentazione, mentre il sovraccarico dei sistemi di proteostasi e l'accumulo di lipofuscina contribuiscono all'opacità e al colorito alterato. Infine, il crosstalk neuro-infiammatorio amplifica ulteriormente questo circolo vizioso. Questo modello integrato sottolinea come la discromia sia un fenomeno sinergico, derivante da un profondo e interconnesso squilibrio del derma.
